外泌体是由各种类型细胞分泌的一种细胞外囊泡,首次发现于绵羊网织红细胞中,而后被命名为exosome,其大小在30~150 nm。在某种刺激下,细胞中晚期内体膜的内向和反向出芽,产生多泡体,而后腔内囊泡聚集后释放即称为外泌体。无论是生理还是病理状态下都可被网织红细胞、树突状细胞、肝细胞、炎性细胞、上皮细胞和肿瘤细胞等多种细胞释放。
起初,外泌体的功能常常被忽视,常常被当作细胞“废物”,但是随着研究技术的提高及科学领域的拓展,研究发现这种所谓的“废物” 在各个领域都充当重要角色,如肿瘤、炎症等方面均是研究热点。
关于间充质干细胞外泌体
间充质干细胞来源的外泌体(MSC-Exo)是由磷脂双分子层包被且腔内充满多种蛋白质、核酸、脂质和可溶性因子的纳米级囊泡,通过细胞膜内陷方式从MSC中释放。MSC-Exo的特殊“脂筏”结构使其表面含有特异蛋白(如CD9、CD63、CD81等),能够直接与靶细胞的质膜融合,还可通过细胞内吞实现信息传递,参与信号转导、炎症因子释放调控、细胞增殖分化调控等过程。
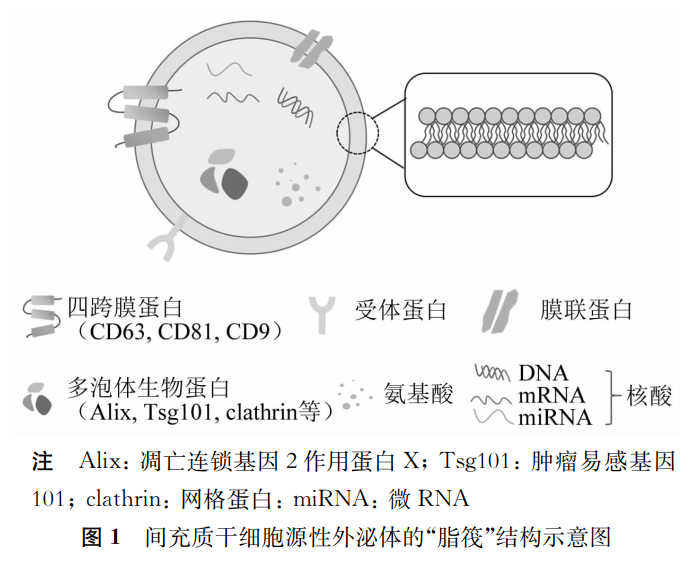
间充质干细胞源性外泌体的“脂筏”结构示意图
相较于MSC,无细胞结构的MSC-Exo易于存储管理,且稳定性更好、免疫原性更低,可有效减少医源性肿瘤的形成和生长,进而降低细胞治疗过程中存在的风险。有研究表明,MSC-Exo可成为替代MSC的无细胞治疗新手段并具有光明前景,目前已在恶性肿瘤、肝脏疾病、心血管及神经退行性疾病、糖尿病等常见疾病的动物模型中对其进行了广泛探究。
全球外泌体监管现状
虽然外泌体在很多疾病的研究中因其潜在的治疗应用而受到广泛关注。然而,由于其独特的细胞内作用机制,其监管环境复杂且在不同国家间存在差异。生产技术的多样性使得其标准化面临挑战,从而导致了碎片化的监管格局。
当前全球的外泌体监管框架可以大致分为两种策略:一种是阐明外泌体中的组成成分,另一种是考察其分泌的生理影响。在将外泌体作为治疗剂使用时,应当像生物药品一样进行管理。与生物制剂类似,外泌体的颗粒大小和蛋白质组成已经被分析。基于外泌体的治疗剂在了解其分子组成和结构,并证明其药代动力学和治疗效果之后,应获得临床批准。
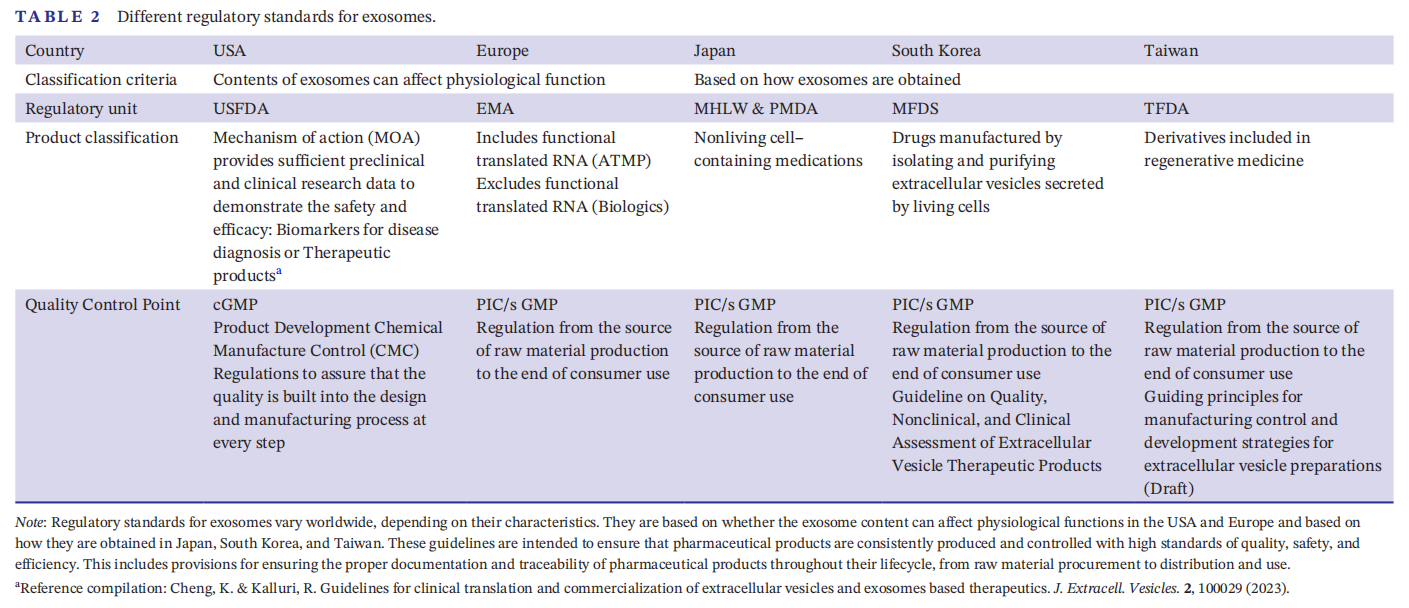
外泌体的监管标准因地区而异,取决于其特性。在美国和欧洲,它们基于外泌体含量是否影响生理功能;在日本、韩国和台湾,它们基于外泌体的获取方式。
美国:
用于治疗人类疾病和状况的外泌体产品根据联邦食品、药物和化妆品法(FD&C 法)作为药物监管,并根据公共健康服务法(PHS 法)作为生物产品监管,需遵循市场前审查和批准要求。
欧洲:
根据欧洲指令(指令 2001/83/EC 和 Regulation 1394/2007/EC),直接从细胞中纯化的外泌体或从转录 RNA 中提取的外泌体不被视为先进治疗药物(ATMPs),而是被归类为生物产品。然而,如果外泌体含有功能性转录 RNA,并且患者在使用后有预期的治疗效果,则这些外泌体被归类为 ATMPs。由欧洲药品管理局(EMA)的先进治疗委员会(CAT)进行评估。
日本:
外泌体在日本被归类为生物制品,需遵守与疫苗、血液制品和其他生物制品相同的监管要求。对于用于医疗的外用制剂,非商业性临床研究由医师逐案管理,因为这些制剂缺乏活细胞成分,不被视为特定加工细胞。
韩国:
韩国食品药品安全部(MFDS)将再生医学相关制剂归类为生物制品,并负责其市场管理。韩国细胞外囊泡学会(KSEV)为外泌体制定的指南提供了开发基于 EV 的产品时需要考虑的质量、非临床和临床方面的要求,并确保其安全性和有效性。因此,这些指南促进了韩国在美容医学领域外泌体的快速发展。然而,到目前为止,没有药用外泌体产品获得市场批准。
我国对外泌体的态度
很长一段时间,外泌体因其超强的综合功能极大地拓展了应用边界,在药、械、妆三界都有着自己独特的作用,但与此同时也正因为它超强的综合实力,而深陷争议之中。
我国对外泌体的态度是谨慎而积极的。国家药监局通过例举欧盟、韩国、日本等化妆品生产国家和地区对人源物质用于化妆品的谨慎态度,说明了中国限制“人源干细胞外泌体”在化妆品行业的应用是基于化妆品安全和伦理的考虑。同时,国家也在积极推动外泌体技术的研发和应用,加强监管框架的完善。

近期,国家药监局医疗器械标准管理中心发布了《2024年第二次医疗器械产品分类界定结果汇总》,其中干细胞外泌体被明确建议不作为医疗器械管理。
既然外泌体在化妆品上的应用受到限制,也不将外泌体作为医疗器械管理,这也就是说官方默认了我国将按照国际主流方式将外泌体按照药品进行监管。

这个答案在意料之中,其实早在2021年国家发改委发布的《十四五生物经济发展规划》中早已给出答案:“外泌体治疗产品”!官方的说法其实也是非常明确外泌体是按药品进行管理。
外泌体按照药品监管,将对其相关的培养耗材、收获设备、鉴定程序等带来诸多挑战,监管机构对于外泌体的严格监管,从某种意义上也将是希望业界对外泌体进行更深入的研究、更规范的临床验证,使得外泌体这种新型物质能够更好地服务大众健康。


 友康生物
友康生物 2024-12-13
2024-12-13 公司热点
公司热点



