2026年4月19日,距离818条例正式实施仅剩11天,国家卫生健康委科教司发布《生物医学新技术临床转化应用审批工作规范(征求意见稿)》(以下简称《工作规范》),作为条例的核心配套细则,在行业内引起了广泛讨论。
在距离五一实施节点如此紧迫的时间下,业内普遍认为,文件的核心框架与关键条款已基本定型,不会有大的变动。其中透露出的监管思路和核心要求,已经足够清晰,值得相关企业高度重视。以下提炼核心要点,简洁明确解读核心要求。
原文链接:https://www.nhc.gov.cn/qjjys/c100015/202604/b4706d6386b046a5bec75050969e6f7f.shtml

一、审批范围:哪些技术可申请?
1. 纳入范围的条件
申请技术须同时满足:
(1)已列入《生物医学新技术临床研究备案指导清单》;
(2)且符合以下两类情形之一:
①个性化程度高,国内尚没有使用同类机制原理的药品获得上市许可或者已启动确证性临床试验;
②用于治疗国家卫生健康委公布的《罕见病目录》收录的罕见病,国内尚没有使用同类机制原理、针对相同适应症的药品获得上市许可或者已启动确证性临床试验。
2. 明确排除的情形
• 符合《医疗器械监督管理条例》定义的医疗器械,应走医疗器械注册路径;
• 已明显具备产品形态、能够标准化规模化生产的药品,应走NMPA药品注册路径。
关键提示:
**“确证性临床试验”作为判断门槛,较此前业内解读的“获得IND批件”的标准有所放宽,为尚未进入III期临床的同类机制药品留出了技术转化空间。
**具备标准化、规模化生产特征的技术(如多数MSC产品)原则上无法进入本通道,除非适应症严格限定于罕见病目录内。
二、申请条件:三大硬性要求
《工作规范》第六条明确,申请临床转化应用须同时具备以下三项条件:

关键提示:
**第3条“多中心独立验证一致”为新增最高门槛,本质上要求技术具备跨机构、跨操作者的可重复性。
**单一中心的IIT数据不再足以作为申请转化应用的充分依据。申请机构须在临床研究阶段即布局至少两家以上独立医疗机构参与确证性验证。
三、审批流程与时限
1.标准流程

总体预估:从提交申请到获得批准,实际耗时约4-7个月。
2.特殊通道
• 优先审查审批:适用于严重危及生命无有效治疗手段、公共卫生急需的技术。申请前可与生物中心沟通,符合要求的可同步提交申请表。
• 紧急应用:应对特别重大突发公共卫生事件时,国家卫生健康委经论证可同意正在临床研究的技术紧急应用,细则另行制定。
四、获批后的管理:限制期与再评估
1. 风险分级与限制期
根据另行制定的《生物医学新技术风险分级指南》划定高、中、低三级风险。获批后设置差异化限制期:

限制期满后,如未触发再评估情形,或再评估证实收益远大于风险,其他符合条件的医疗机构方可申请使用。
关键提示:
**此设计系“渐进式推广”机制,目的是在可控范围内收集真实世界数据,控制远期风险。
**技术获批不等于立即全国推广。申请机构需做好限制期内的有限商业化准备及长期随访投入。
2. 再评估与退出机制
触发再评估的四种情形:
(1)科学认识发展,对技术安全性、有效性有新的判断;
(2)临床应用中出现严重不良反应或不可控风险;
(3)造成重大社会稳定风险或事件;
(4)国家卫健委规定的其他情形。
再评估期间暂停技术应用。评估内容包括安全有效性评估及卫生经济学评估(与适应症相同的药品、医疗器械对比)。经评估不能保证安全有效的,国家卫健委将禁止临床应用并公布。
关键提示:
**审批并非一劳永逸,而是全生命周期动态管理。
**卫生经济学评估的引入意味着,即使技术安全有效,若性价比显著劣于已有替代方案,仍可能面临叫停风险。
五、多中心独立验证的技术实现路径
“多中心独立验证一致”是整份规范中对行业操作层面影响最大的条款之一。其核心要求是:技术在不同机构、由不同操作者实施时,必须得到一致的安全性和有效性结论。这本质上是对技术可重复性、工艺稳健性和操作标准化的综合检验。
1. 多中心验证面临的主要技术挑战
(1)设备与环境差异:不同医疗机构的实验室设备型号、洁净环境等级、检测仪器校准状态存在差异,可能影响细胞制备和质控结果的一致性。
(2)操作人员差异:手工操作依赖个人经验,不同技术员在细胞换液、接种密度、培养时间等环节的微小差异可能累积为批次间偏差。
(3)数据可追溯性要求:文件附录明确要求提交“历次临床研究记录及临床研究数据库”。手工记录难以满足全流程、不可篡改的数据审计要求。
(4)技术输出难度:由于《专利法》规定疾病诊疗方法不授予专利权,获批后操作规范须公开。若技术高度依赖特定设备或特定人员经验,其他机构难以准确复现。
2. 自动化工作站在满足多中心验证要求中的作用


简要结论:
在多中心验证成为强制性前置条件的监管框架下,自动化工作站是实现“跨中心、跨操作者、结果一致”的工程化工具之一。其价值在于将依赖个人经验的“手艺”转化为可编程、可复制的标准化流程,从而满足监管对技术可重复性的底层要求。
以友康生物的全自动细胞培养工作站为例,其设计思路正是针对行业痛点:
1.全封闭系统,终结污染风险。设备配套管路系统均为一次性预灭菌耗材,在A级生物安全柜完成对接后,整个培养过程在全封闭环境中自动运行,对外部环境要求低,无需人工干预。与传统手工培养需要数十次开放式操作相比,污染风险降低90%以上。
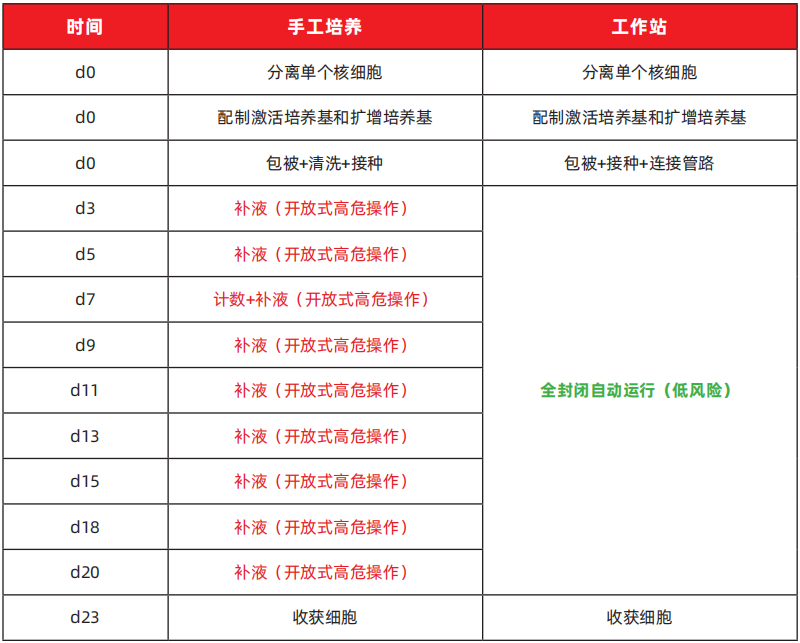
2.程序化控制,确保批次稳定。设备将细胞培养的每一个步骤转化为可重复的程序,试剂保存区保持2-8℃恒温,培养箱维持37℃、5% CO₂的稳定环境,非接触式密度监测模块实时监测细胞生长并自动调整补液策略。
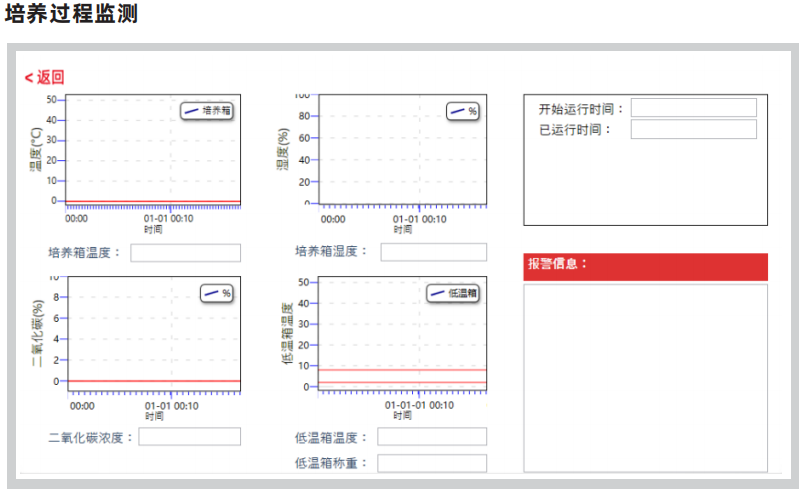
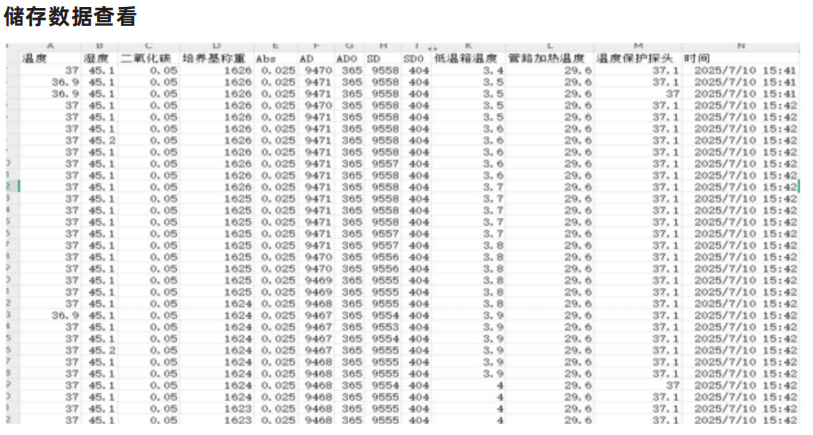
3.数据全程记录,满足追溯要求。操作数据实时自动记录、不可篡改,完整覆盖培养全流程。对于需要推进多中心临床研究的企业而言,这样的设备可以为监管审计提供完整、可追溯的工艺数据。
YOCON
总体而言,《工作规范》作为818号令的核心配套文件,其制度价值体现在三个层面:
第一,首次为“非药品路径”的生物医学新技术建立了国家级的行政审批通道,结束了过去IIT完成后无路可走或只能灰色推广的局面;
第二,与NMPA药品注册路径共同构成清晰的“双轨制”监管格局,技术归卫健委、产品归药监局,企业可据此在项目立项阶段做出明确的路径选择;
第三,通过“多中心独立验证”、“风险分级限制期”、“再评估与退出机制”等制度设计,构建了一套覆盖申请、审批、应用、退出的全生命周期监管闭环。
这份文件的出台,标志着我国生物医学新技术监管从“以备案为主的事前管理”转向“以审批为核心的全链条管理”,行业自此进入有法可依、有章可循的规范化发展阶段。
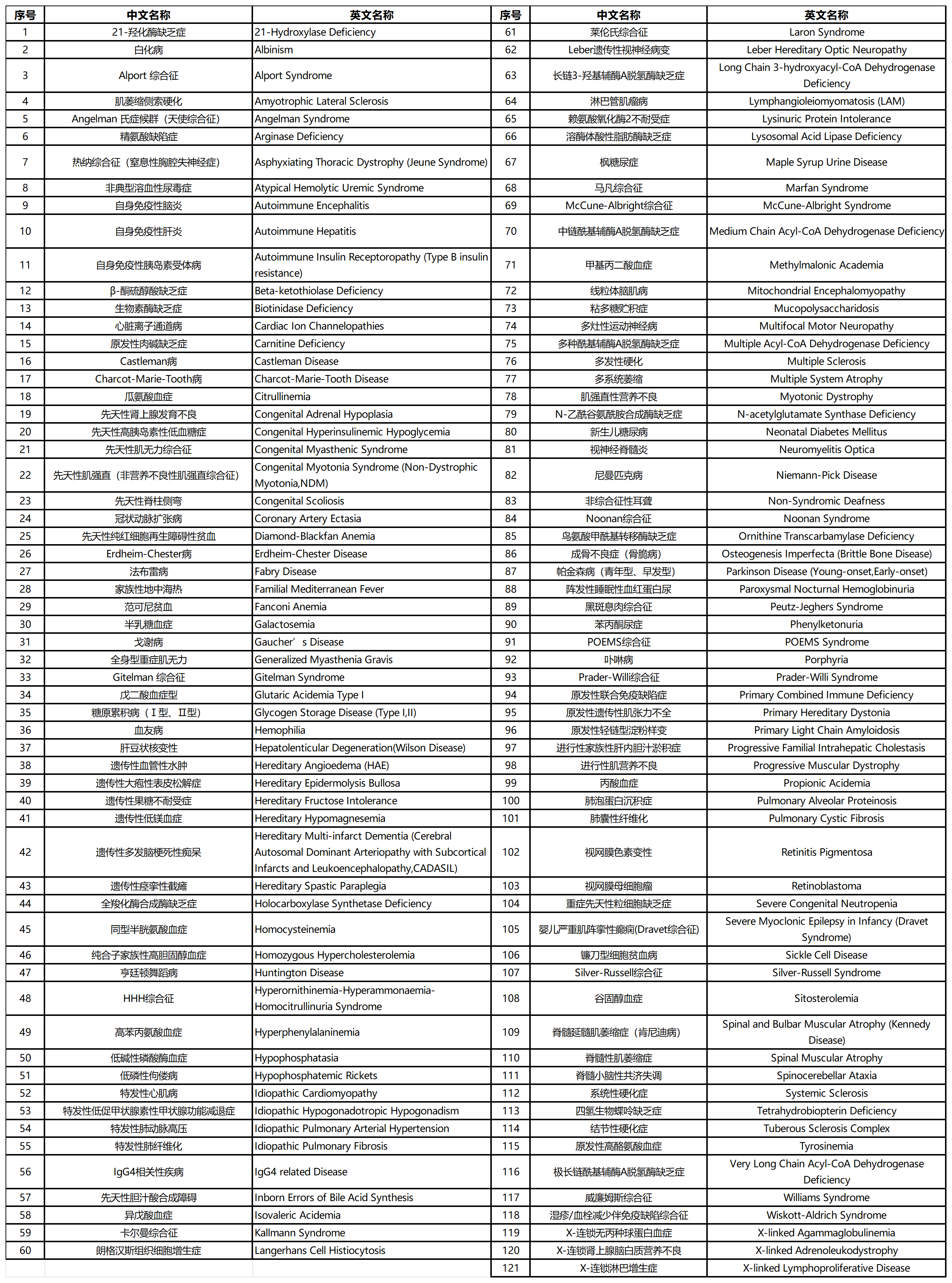
国家卫生健康委公布的《罕见病目录》

 友康生物
友康生物 2026-04-20
2026-04-20 行业热点
行业热点



